文章转载自精准细胞治疗之家
时光总是匆匆易逝,这不,12月马上就要开始了,而2016年也已经接近尾声,迎接我们的将是崭新的2017年,2016年三大国际著名杂志Cell、Nature和Science(CNS)依然刊登了很多亮点耐人寻味的研究,本文中小编就盘点了2016年Science杂志发表的一些非常有意义的重磅级亮点研究,与各位一起学习!
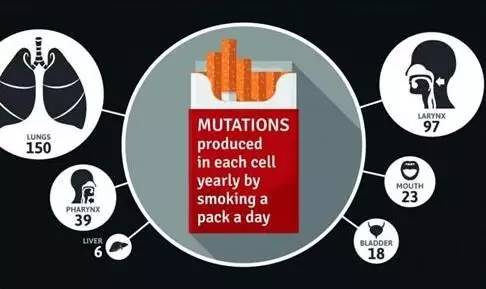
【1】Science:重磅!每天抽一包烟导致肺细胞每年产生150种突变
doi:10.1126/science.aag0299
在一项新的研究中,来自英国剑桥大学韦尔科姆基金会桑格学院研究所和美国洛斯阿拉莫斯国家实验室的研究人员和他们的合作者测量了吸烟在人体不同器官中导致的灾难性遗传损伤,鉴定出吸烟导致DNA突变的几种不同机制。他们发现对每天吸一包烟的吸烟者而言,这些吸烟者的每个肺细胞每年积累着平均150个额外的突变。相关研究结果发表在2016年11月4日那期Science期刊上,论文标题为“Mutational signatures associated with tobacco smoking in human cancer”。
这项研究提供一生当中抽的香烟数量与人肿瘤DNA中的突变数量之间存在的直接关联性。最高的突变率是在肺癌中观察到的,但是人体其他部分的肿瘤也含有这些与吸烟相关的突变,这就解释了吸烟如何导致很多种类型的人类癌症。
吸烟每年夺走至少600万人的生命,而且如果当前的趋势继续持续下去的话,那么世界卫生组织预计在这个世纪会有10亿例与吸烟相关的死亡。在流行病学上,吸烟与至少17种人类癌症相关联,但是在此之前没有人观察到吸烟导致许多这些癌症类型产生的机制。
【2】Science:科学家揭示HIV广泛中和抗体3BNC117的强效作用
doi:10.1126/science.aaf0972 doi:10.1126/science.aaf1279
多年以来,科学家们在治疗HIV感染时一直面临一个棘手的问题:HIV在人体中变异迅速,随着时间的推移,将会减少治疗的有效性。
再者,开发出的抗逆转录病毒药物(ARV)---延缓HIV体内复制的药物组合---已极大地改变了对HIV感染的治疗。曾经一度被宣判为死刑的HIV感染如今变成一种慢性疾病:病人能够携带HIV存活数十年。
但是这种疗法也有不足之处。它的副作用包括肾脏问题、骨密度下降和胃肠道问题。如果一个人停止他或她的治疗,甚至只是少服用几剂药物,人体内的HIV病毒水平就能够快速反弹。
来自美国洛克菲勒大学分子免疫学实验室的Michel Nussenzweig团队在2011年从一名HIV感染者---这名感染者的免疫系统通过阻止HIV感染和破坏一种特定的被称作CD4 T细胞的免疫细胞而能够很好地中和血液中的HIV---体内分离出一种新型的HIV广泛中和抗体3BNC117。
在第一项发表在2015年6月25日那期Nature期刊上的研究中,Nussenzweig团队发现在29名受试者中检测了4种不同剂量的3BNC117;受试者中有17人携带HIV,其中有15人没有服用ARV药物。给其中8人注射了最高剂量(每公斤体重30毫克)的3BNC117,一周后大多数受试者体内的病毒量达到最低水平;28天后,受试者血液中的病毒量分别降低了8~250倍。病毒载量下降的程度取决于受试者起始的病毒载量以及个人携带的HIV病毒株对3BNC117的敏感性。
【3】Science:重磅!史上首次利用CRISPR-Cas9让人细胞变身为记忆存储系统
doi:10.1126/science.aag0511
在一项新的研究中,来自美国麻省理工学院(MIT)的研究人员设计出一种方法在人细胞的DNA中记录复杂的历史事件,从而允许他们通过对这种DNA进行测序从中找回过去事件的“记忆”。相关研究结果于2016年8月18日在线发表在Science期刊上,论文标题为“Continuous genetic recording with self-targeting CRISPR-Cas in human cells”。论文通信作者为MIT电学工程与计算机科学副教授和生物工程副教授Timothy Lu。论文第一作者为Samuel Perli博士和研究生Cheryl Cui。
这种模拟记忆储存系统---首先能够在人细胞中记录事件的持续时间和/或强度---可能也能够允许科学家们研究干细胞在胚胎发育期间如何产生多种组织,细胞如何对环境条件作出反应以及它们如何发生导致疾病产生的基因变化。
Lu说,“为了能够更加深入地理解生物学,我们对人细胞进行基因改造,使得它们能够基于基因编码的记录器报道它们自己的历史事件。”他补充道,这种技术应当允许深入认识基因调节和细胞内发生的其他事件如何导致疾病产生和发育。
【4】Science:重磅!改写教科书上的共生经典例子
doi:10.1126/science.aaf8287
地衣(lichen)的词典条目可能需要编辑一下。一项新的研究推翻了关于地衣的古老的一种藻类-一种真菌共生观点,替换它的是一种略微复杂的观点:一种藻类-两种真菌,其中这两种真菌为已知的子囊菌和新发现的担子菌酵母。相关研究结果于2016年7月21日在线发表在Science期刊上,论文标题为“Basidiomycete yeasts in the cortex of ascomycete macrolichens”。
论文共同作者、美国普渡大学真菌学家M. Catherine Aime在新闻稿中说,“这一发现推翻了我们关于地球上这种研究得最为透彻的共生关系的长期假设。这些酵母组成一个完整的但是之前不为人所知的群体,但是它们作为第三种共生伙伴存在于每个大陆上的许多种地衣中。”
【5】Science:忘记PD-L1吧,破坏Cdk5也能促进抗肿瘤免疫反应
doi:10.1126/science.aae0477
肿瘤通常利用类似于在健康细胞表面上发现的那些蛋白的蛋白进行自我修饰,从而躲避免疫检测。这种防护罩允许它们不被检测地生长,因而经常产生致命性的结果。根据美国脑瘤协会的统计数据,脑瘤每年导致大约1.7万例死亡病例,同时每年新增4600多名儿童脑瘤确诊病例。
通过协调一系列蛋白信号,肿瘤细胞调节它们的防护罩。这些信号通常处于被称作丝氨酸/苏氨酸蛋白激酶的中枢协调蛋白的控制之下。
在一项新的研究中,来自美国凯斯西储大学医学院的研究人员研究了一种被称作周期蛋白依赖性激酶5(Cdk5)的关卡蛋白,它也是一种在神经细胞和肿瘤细胞发展中起着至关重要的丝氨酸/苏氨酸蛋白激酶。他们特地研究Cdk5在成神经管细胞瘤(medulloblastoma)---一种常见的生长迅速的儿童脑瘤---发展中的作用。他们发现这种关卡蛋白允许某些脑瘤细胞(如成神经管细胞瘤)躲避免疫系统检测。相关研究结果发表在2016年7月22日那期Science期刊上,论文标题为“Cdk5 disruption attenuates tumor PD-L1 expression and promotes antitumor immunity”。论文通信作者为凯斯西储大学医学院儿科学、病理学与生物医学工程副教授Alex Huang博士和儿科学助理教授Agnes Petrosiute博士。
【6】Science:深入探究新型HIV药物的作用机制
doi:10.1126/science.aaf9620
日前,刊登于国际杂志Science上的一篇研究报告中,来自欧洲分子生物学实验室和海德堡大学医院的研究人员正在利用一种特殊的方法来检测一种新型的HIV药物,同时研究者还发现,但病毒开始对早期的药物产生抗性时,其并不会阻断或者抑制药物的效应,而是会绕过这些药物来感染机体。
文章中,研究者就描述了不成熟的HIV的详细作用机制;HIV包括两种形式:成熟病毒颗粒和未成熟病毒颗粒,不成熟的病毒颗粒实在感染个体的细胞中进行组装的,当未成熟的病毒颗粒离开细胞后,其在感染其他个体之前必须改变成为成熟的形式,当前研究者正在对一类新型药物进行临床试验,这类药物就可以抑制病毒的成熟过程,但截止到目前为止科学家并不清楚这种药物的作用机制。
【7】Science:史上首次!揭示为何父本线粒体在受精后不会遗传给后代
doi:10.1126/science.aaf4777
半个世纪以来,人们就已了解到一些数量的DNA存在细胞核外的线粒体中。线粒体在细胞过程中发挥着至关重要的作用,提供让细胞正常运转的呼吸功能和代谢功能。
人们还发现在几乎所有动物的繁殖期间,只有母本线粒体DNA传递给后代,而父本线粒体DNA在它发挥影响之前就在受精卵中被选择性地摧毁了。这个过程背后的精确机制一直是不清楚的。谈及线粒体遗传时,为何母体基因是以牺牲父本基因的代价来发挥统治力呢?
在一项新的研究中,来自中国、美国和日本的研究人员针对这个长期存在生物学秘密,描述了他们在卵子被受精后立即对父本线粒体DNA进行密切监控,研究了它为何随后被摧毁。他们发现精子线粒体DNA在进入胚胎中后,在自噬体(autophagosome)开始接触和切割它之前,就已开始自我摧毁。相关研究结果于2016年6月23日在线发表在Science期刊上,论文标题为“Mitochondrial endonuclease G mediates breakdown of paternal mitochondria upon fertilization”。论文通信作者为来自中国香港中文大学的Byung-Ho Kang和来自美国科罗拉多大学博尔德分校的Ding Xue。
【8】Science:重大进展!破解免疫系统秘密有助治疗一系列疾病
doi:10.1126/science.aad1210
在一项新的研究中,来自美国、英国、德国和爱尔兰的研究人员揭示出我们古老的免疫系统的秘密。这一重大的科学进步可能有助全球的科学家和临床医生抵抗疾病。相关研究结果发表在2016年6月17日那期Science期刊上,论文标题为“T helper 1 immunity requires complement-driven NLRP3 inflammasome activity in CD4+ T cells”。
论文共同作者、澳大利亚昆士兰大学分子生物科学研究所教授Matt Cooper博士说,免疫系统基本上可分为两个部分:适应性免疫系统,产生抵抗感染的抗体;非常古老的先天性免疫系统。
在此之前,科学家们之前总是认为适应性免疫反应和先天性免疫反应的关键组分,独立发挥作用,即巨噬细胞和树突细胞等先天性免疫细胞识别入侵的微生物,然后给T细胞等适应性免疫细胞发出警报,接着这些适应性免疫细胞作出反应,从而杀死入侵的微生物。
【9】Science:重大发现!从结构上揭示基因特异性转录激活蛋白工作机制
doi:10.1126/science.aaf4417
在一项新的研究中,来自美国罗格斯大学的研究人员发现一种基因特异性转录激活复合物的三维结构,并且首次在结构上和机制上描述了细胞用来开启或者说激活特异性基因以应对细胞形状、发育状态和环境的变化的过程。相关研究结果发表在2016年6月10那期Science期刊上,论文标题为“Structural basis of transcription activation”。
转录是细胞采取一系列步骤读取DNA中遗传信息的第一步。
在这项研究中,来自罗格斯大学的Richard Ebright、Yu Feng和Yu Zhang证实一种转录激活蛋白(transcription activator protein, 也译作转录激活因子)如何与细胞用来进行转录的RNA聚合酶相互作用。他们也证实这种转录激活蛋白如何协助RNA聚合酶在基因前面的特异性位点上结合到DNA双螺旋上,以及这种转录激活蛋白如何协助RNA聚合酶让DNA双螺旋解旋从而启动基因转录。
【10】Science:基因编辑大牛张锋再发力,揭示只靶向RNA的新型CRISPR系统
doi:10.1126/science.aaf5573
在一项新的研究中,来自美国国家卫生研究院(NIH)、哈佛大学-麻省理工学院布罗德研究所(简称布罗德研究所)、麻省理工学院、罗格斯大学新伯朗士威校区和俄罗斯斯科尔科沃理工学院等机构的研究人员描述了一种靶向作用于RNA而不是DNA的新型CRISPR系统。相关研究结果于2016年6月2日在线发表在Science期刊上,论文标题为“C2c2 is a single-component programmable RNA-guided RNA-targeting CRISPR effector”。
这种新的CRISPR系统有潜力提供一种强大的方法进行细胞操纵。尽管DNA编辑让细胞基因组发生永久性变化,但是这种基于CRISPR的RNA靶向方法可能允许科学家们让细胞基因组发生可根据需要进行上下调节的临时变化,而且比现存的RNA干扰方法具有更大的特异性和功能性。
在这项研究中,来自布罗德研究所的张锋(Feng Zhang)及其同事们与来自NIH的Eugene Koonin及其同事们、来自罗格斯大学新伯朗士威校区的Konstantin Severinov等组成一个合作小组,鉴定出一种RNA引导的能够靶向结合和降解RNA的酶C2c2,并对C2c2进行功能性描述。

【11】Science:首次开发出基因组编辑技术GESTALT追踪细胞谱系
doi:10.1126/science.aaf7907
根据一项新的研究,在经过基因改造的斑马鱼胚胎中让特定的人工合成DNA片段发生突变能够让研究人员不可逆地对发育期间的细胞和它们的子细胞进行标记。这种技术允许沿着成体细胞谱系图追踪到它们的胚胎起源。相关研究结果于2016年5月26日在线发表在Science期刊上,论文标题为“Whole organism lineage tracing by combinatorial and cumulative genome editing”。
这些作者“开发出一种非常强大的工具而允许我们对细胞和器官发育进行谱系追踪。” 美国南加州大学干细胞生物学家Rong Lu(未参与这项研究)说。“我认为研究癌症等疾病和理解组织再生也是非常有趣的”,她说。
发育生物学的最重要---如果还没有确定的话---目标是理解单个受精卵如何发育成一个完整的多细胞有机体。基本上,发育生物学家想知道“一种给定的细胞变成什么,以及它何时进行这样的转变”,美国约翰霍普金斯大学医学院遗传学家Aravinda Chakravarti(未参与这项研究)说。
【12】Science:癌症免疫疗法重大突破,利用他人的T细胞抵抗癌症
doi:10.1126/science.aaf2288
在一项新的研究中,来自荷兰癌症研究所、挪威奥斯陆大学和丹麦哥本哈根大学的研究人员在癌症免疫疗法上取得新的突破,他们证实即便一个人自己的T细胞(一类免疫细胞)不能够识别和抵抗他们自身的肿瘤,但是其他人的T细胞可能会做到这点。相关研究结果于2016年5月19日在线发表在Science期刊上,论文标题为“Targeting of cancer neoantigens with donor-derived T cell receptor repertoires”。
这项研究证实将来自癌细胞的发生突变的DNA加入到来自健康供者的T细胞中能够让健康供者的T细胞产生免疫反应。在将来自这些供者T细胞的特定组分导入回到癌症病人的T细胞中后,研究人员能够让癌症病人自己的T细胞识别癌细胞。
作为一个快速发展的领域,癌症免疫疗法旨在开发让人体自己的免疫系统抵抗癌症的技术。有多种可能的原因能够阻止T细胞识别癌细胞。首先,T细胞的活性受到很多能够干扰它们功能的抑制因素的控制,而且让这些抑制因素失效的疗法如今正在很多人类癌症中开展测试。其次,在一些病人体内,免疫系统可能并不会在第一时间将癌细胞作为异常细胞加以识别。也因此,帮助免疫系统更好地识别癌细胞是癌症免疫疗法的主要目标之一。

【13】Science新研究为几十年争论提供新证据 找到记忆形成重要基石
DOI: 10.1126/science.aad5252
几十年来,科学家们对于快速眼动睡眠是否直接参与记忆形成争论不休。现在一项发表在国际学术期刊Science上的最新研究表明,快速眼动睡眠确实在记忆形成过程中发挥一定作用--至少在小鼠模型上确实是这样。
这项研究由麦吉尔大学和伯尔尼大学的研究人员共同完成。该研究首次证明快速眼动睡眠对于小鼠正常的空间记忆形成过程具有非常重要的作用。
之前大量研究使用传统实验方法都未能对快速眼动睡眠期的神经活动进行分离。而在这项最新研究中,研究人员使用了光遗传技术,该技术能够精确靶向神经元群体,通过光控制神经元活动。
【14】Science:首次在活体细胞中观察到单个mRNA分子的翻译过程
doi:10.1126/science.aaf1084
近日,刊登在国际杂志Science上的一项研究报告中,来自爱因斯坦医学院 ( Albert Einstein College of Medicine)的研究人员利用一种特殊技术在活体哺乳动物细胞中首次观察到了翻译成为蛋白质的单个信使RNA分子(mRNA),这对于后期科学家们进行神经变性疾病及癌症等多种人类疾病的研究或将带来一定思路。
研究者Robert Singer表示,翻译是机体中将mRNA信息转化成为蛋白质的基本过程,通过全基因组研究我们知道,转录可以控制细胞中蛋白质的水平,而细胞中蛋白质的丰度对于细胞功能的发挥非常重要,利用新型技术研究人员最终揭示了调节蛋白质翻译的机制,同时也为深入解析疾病发病机制提供了一定研究数据。
文章中研究人员首次在人类骨肉瘤癌细胞和小鼠神经元细胞中观察到了单个mRNA的翻译情况,尤其是在小鼠神经元中,研究者发现了mRNA翻译的一种前所未有的现象。神经元可以非常紧密地控制蛋白质的合成,因为神经传输依赖于在突触中蛋白质的精确合成,而在突触位置神经元就可以形成回路。翻译活性的爆发或许可以帮助神经元有效控制蛋白产生的水平和位置,因此这项研究对于揭示诸如脆性X染色体综合征等智力障碍的发病机制非常关键。