最新一期著名期刊《科学》杂志发表一篇来自斯坦福大学医学院的重磅文章,研究者们开发出一种利用突变IL2(orthoIL-2)以及相应的IL2突变受体β(orthoIL-2Rβ)来特异性地在体内扩增包括CAR-T在内的过继性T细胞的方法,能够有效地避免直接注射IL-2引起的巨大副作用。
白介素2(Interleukin-2,IL-2)对于T细胞的增殖、维持以及功能具有关键作用,其对于包括CAR-T在内的过继性T细胞免疫治疗也具有重要作用。
如今,过继性T细胞(adoptive T cell transfer,ACT)疗法在肿瘤治疗方面已经取得里程碑式进展,尤其是嵌合抗原受体T细胞(chimeric antigen receptor T cell,CAR-T)疗法,目前已经有目前已经有诺华的Kymriah以及Kite公司(现已被吉列德公司收购)的Yescarta上市。
▲全球首款上市的CAR-T产品,诺华公司的Kymriah(图片来自网络)
然而,过继性T细胞移植(ACT)疗法广泛应用于治疗癌症有几个局限性,包括产生足够量的输注细胞以及输入的过继性T细胞未能持续并在体内保持功能。
由于白介素2(Interleukin-2,IL-2)对于T细胞的增殖、维持以及功能具有关键作用,因此,在临床中,T细胞生长因子白细胞介素-2(IL-2)的伴随给药改善了移植的T细胞的存活,功能和抗肿瘤活性【1,2】。
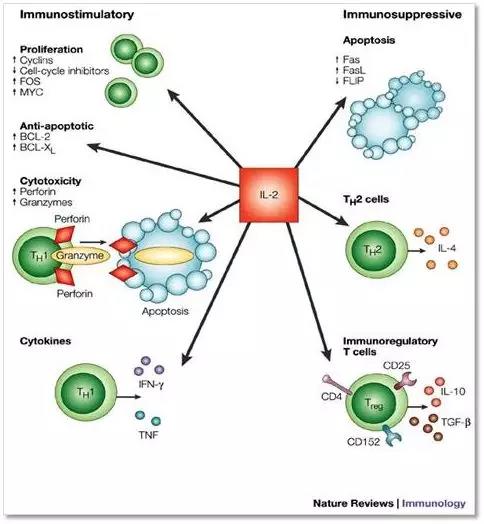
▲白介素-2具有广泛的作用(图片来自Nature)
然而,IL-2的作用非常广泛,除了上面说的维持活化的T细胞增殖以外,其诱导CTL、NK和LAK等多种杀伤细胞的分化和效应功能,并诱导杀伤细胞产生IFN-γ、TNF-α等细胞因子,以及直接作用于B细胞,促进其增殖、分化和Ig分泌等等。
这样一来,使用IL-2来增强包括CAR-T在内的过继性T细胞移植就具有潜在的严重毒性【3】。
这种IL-2的毒副作用是由于IL-2与IL-2受体(IL-2R)之间的相互作用决定【4】。IL-2受体(IL-2R)由α,β和γ这三个亚基组成,而IL-2R的β链(IL-2Rβ)和普通γ链(IL-2Rγ)一起形成信号二聚体并以中等亲和力与IL-2结合,而IL-2Rα(CD25)不发出信号但增加IL-2与IL-2Rβγ的亲和力,从而使T细胞对低浓度IL-2敏感。
因此,有没有办法来改进呢?

▲研究者们在《科学》杂志上面发表的文章(图片来自Science)
最新一期著名期刊《科学》杂志发表一篇来自斯坦福大学医学院的重磅文章,研究者们开发出一种利用突变IL2(orthoIL-2)以及相应的IL2突变受体β(orthoIL-2Rβ)来特异性地在体内扩增包括CAR-T在内的过继性T细胞的方法,能够有效地避免直接注射IL-2引起的巨大副作用【5,6】。
▶锁和钥匙◀
既然IL-2对于细胞免疫疗法如此重要,可以说不用IL-2就不行,然而用了IL-2又会有巨大的副作用,那怎么办呢?
这正是这篇由斯坦福大学医学院发表的《科学》文章要解决的事情。
这篇文章具体是怎么回事呢?

▲可以把过继性T细胞(或者CAR-T细胞)比喻成门,而在其表面的IL-2R(α、β以及γ亚基)可以比喻成锁,IL-2可以比喻成钥匙;因此,一把钥匙配一把锁,野生型的IL-2只能结合野生型的IL-2R;而突变型的IL-2就只能够结合相应的突变型的IL-2R(图片来自网络)
既然这种IL-2的毒副作用是由于IL-2与IL-2受体(IL-2R)之间的相互作用决定的,因此,研究者们就在这IL-2以及IL-2R上面来下功夫。
先来打个不是特别恰当的比喻,可以把过继性T细胞(或者CAR-T细胞)比喻成门,而在其表面的IL-2R(α、β以及γ亚基)可以比喻成锁,IL-2可以比喻成钥匙;因此,一把钥匙配一把锁,野生型的IL-2只能结合野生型的IL-2R;而突变型的IL-2(在文章中以orthoIL-2表示)就只能够结合相应的突变型的IL-2R(在文章中以orthoIL-2Rβ表示)。
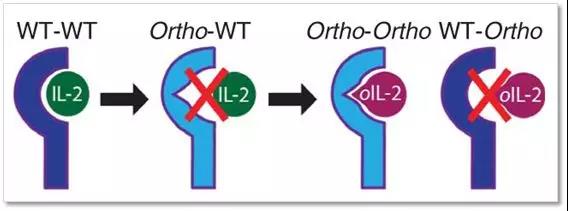
▲一把钥匙配一把锁,研究者们先把IL-2R(锁)进行突变,获得突变的IL-2R(用ortho表示)(图片来自Science)
因此,研究者们首先改造IL-2R,也就是门上面的“锁”,将IL-2R进行突变,使之不能够结合正常的(野生型)的IL-2。
这就好比把门上的“锁”先换掉,然后再根据这个新锁来配新的钥匙。
因此,得到新锁之后,研究者们就来配相应的钥匙了。所以,研究者们通过酵母展示技术来筛选与突变的IL-2R(用orthoIL-2Rβ表示,主要是突变β链)相应的突变型IL-2(用orthoIL-2表示)。
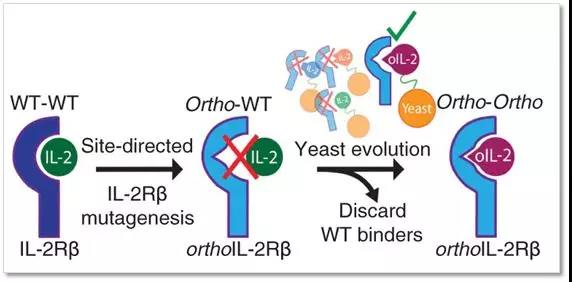
▲研究者们先把IL-2R(锁)进行突变,获得突变的IL-2Rβ(用ortho表示),然后使用酵母展示技术来筛选与突变IL-2Rβ(orthoIL-2Rβ)相应的突变IL-2(orthoIL-2)(图片来自Science)
▶安装◀
有了新的钥匙和锁之后,接下来就是如同搬新家一样,把新的锁安装到门上,然后用新的钥匙开门就行了。
怎么做呢?
很简单,先将orthoIL-2Rβ在过继性T细胞疗法比如CAR-T细胞中表达,这样一来,T细胞表面的orthoIL-2R(其胞内的结构域仍然保留)只能够与orthoIL-2结合而不能与正常的IL-2结合,从而刺激T细胞中的STAT5的磷酸化,从而促进T细胞增殖及维持其活性。
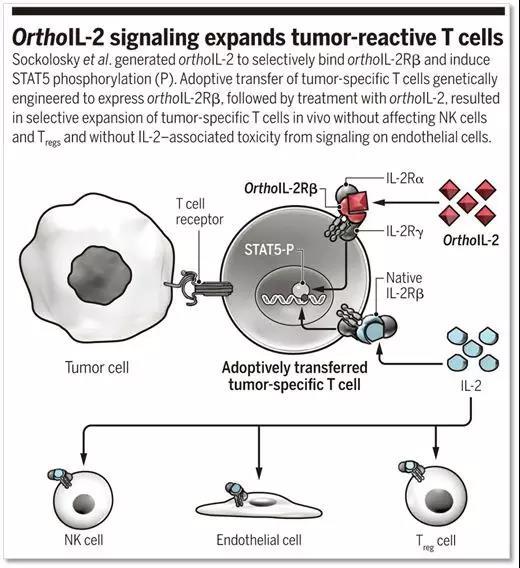
▲《科学》杂志同期评论文章的示意图,将orthoIL-2Rβ在过继性T细胞疗法比如CAR-T细胞中表达,这样一来,T细胞表面的orthoIL-2R(其胞内的结构域仍然保留)只能够与orthoIL-2结合而不能与正常的IL-2结合,从而刺激T细胞中的STAT5的磷酸化,从而促进T细胞增殖及维持其活性(图片来自Science)
换了新的锁和钥匙之后,这意义就比较大了。以前,向患者体内输入了CAR-T之后治疗肿瘤,然后再注射一针IL-2来维持CAR-T细胞在体内的较长时间停留(此处未必严谨),然而,这会造成强烈的免疫反应和副作用,因此,IL-2不能乱用。而这里,在移植了过表达orthoIL-2R的CAR-T细胞之后,只需要再注射orthoIL-2来维持CAR-T细胞在体内的较长时间存在就可以了,也不用担心副作用了,因为orthoIL-2是突变的IL-2,不能够刺激其他免疫细胞的反应。
▶效果如何◀
事实也是如此,一些免疫反应指标在使用了orthoIL-2之后均未增加。
注射orthoIL-2(ortho1G12以及ortho3A10两个突变体)之后,与注射PBS差不多,脾脏重量也未增加(D),CD8 MP(E)、CD4 Treg(F)以及NK细胞(G)均未增加,而正常的IL-2则能够促使上述指标均大幅增加。这表明orthoIL-2不会引起强烈的免疫反应。
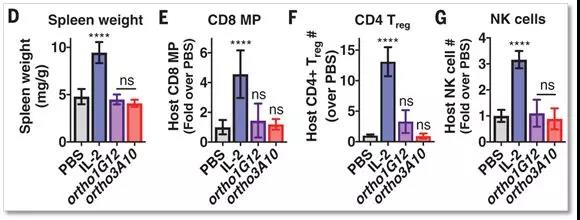
▲注射orthoIL-2(ortho1G12以及ortho3A10两个突变体)之后,与注射PBS差不多,脾脏重量也未增加(D),CD8 MP(E)、CD4 Treg(F)以及NK细胞(G)均未增加,而正常的IL-2则能够促使上述指标均大幅增加(图片来自Science)
当然,说的这么好,关键是这个新方法对于肿瘤的治疗效果如何呢?
可以说,治疗效果还是不错的。
能够有效地控制肿瘤的大小,而且,能够现住地提高荷瘤小鼠的生存率。
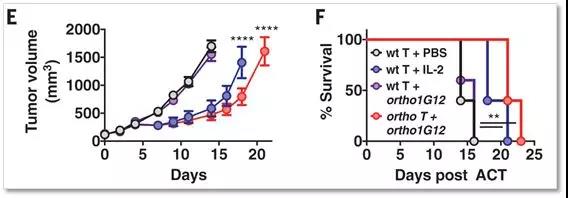
▲新方法能够控制肿瘤的大小(E)以及提高荷瘤小鼠的生存率(F);红色组表示新方法的实验结果(图片来自Science)
“这些结果为使用基因工程表达orthoIL-2Rb的肿瘤特异性T细胞检测过继性细胞疗法铺平了道路。”斯坦福大学肿瘤中心的肿瘤学家Crystal L. Mackall在《科学》杂志上评论说。
她进一步指出:“这些结果具有广泛的临床应用潜力,因为它们提供了令人信服的证据表明这套细胞因子系统可以有效地用于癌症免疫治疗。”
![]()
参考资料:
1. Adoptive T cell therapy using antigen-specific CD8+ T cell clones for the treatment of patients with metastatic melanoma: In vivo persistence, migration, and antitumor effect of transferred T cells. Proc. Natl. Acad. Sci. U.S.A. 99, 16168–16173 (2002).
2. Long-lasting complete responses inpatients with metastatic melanoma after adoptive cell therapy with tumor-infiltrating lymphocytes and an attenuated IL2 regimen. Clin. Cancer Res.22, 3734–3745 (2016).
3. IL-2: The first effective immunotherapy for human cancer. J. Immunol. 192, 5451–5458 (2014).
4. Structure of the quaternary complex of interleukin-2 with its α , β , and γ c receptors. Science 310, 1159–1163(2005).
5. Selective targeting of engineered Tcells using orthogonal IL-2 cytokine-receptor complexes.2018.
6. Engineering a designer immunotherapy.2018.